Liệu pháp tế bào CAR-T – Bước tiến mới trong điều trị ung thư máu
Liệu pháp tế bào CAR-T là một liệu pháp mới trong điều trị ung thư máu bắt đầu triển khai tại Hoa Kỳ từ năm 2017. Tại Việt Nam, các đơn vị, trong đó có Viện Huyết học – Truyền máu TW, đang nỗ lực hợp tác quốc tế để làm chủ công nghệ và giảm chi phí, tăng cơ hội tiếp cận cho người bệnh trong tương lai.
Trong hơn một thập kỷ qua, y học ung thư học đã chứng kiến sự xuất hiện của các liệu pháp miễn dịch đột phá, trong đó liệu pháp tế bào CAR-T (Chimeric Antigen Receptor T-cell) được xem là bước ngoặt trong điều trị các bệnh ung thư huyết học kháng trị. Liệu pháp này khai thác khả năng nhận diện và tiêu diệt tế bào ung thư của hệ miễn dịch, bằng cách tái lập trình tế bào lympho T của chính bệnh nhân để chúng có thể nhận diện đặc hiệu kháng nguyên bề mặt của tế bào ác tính.
Kể từ khi sản phẩm CAR-T đầu tiên được Cục Quản lý Dược và Thực phẩm Hoa Kỳ (FDA) phê duyệt năm 2017, lĩnh vực này đã phát triển mạnh mẽ với hàng nghìn thử nghiệm lâm sàng trên toàn cầu và nhiều sản phẩm thương mại hóa thành công, mở ra hy vọng điều trị triệt để cho các thể ung thư từng được coi là “kháng trị tuyệt đối”.
Về cơ chế tác dụng, liệu pháp CAR-T được thực hiện qua quy trình gồm nhiều giai đoạn chặt chẽ. Đầu tiên, tế bào T của bệnh nhân được thu thập bằng phương pháp leukapheresis, sau đó được chuyển gen để biểu hiện một thụ thể tổng hợp – chimeric antigen receptor (CAR) – có khả năng gắn với kháng nguyên đặc hiệu trên bề mặt tế bào ung thư, điển hình là CD19 trong các bệnh lý tế bào B.
Thụ thể CAR có cấu trúc gồm ba vùng chức năng chính: vùng nhận diện kháng nguyên ngoại bào (single-chain variable fragment – scFv), vùng xuyên màng (transmembrane domain) và vùng nội bào kích hoạt tín hiệu (endodomain) chứa CD3ζ -CD3 zeta chain cùng các yếu tố đồng kích thích như CD28 hoặc 4-1BB, giúp tăng cường tín hiệu hoạt hóa và kéo dài thời gian sống của tế bào T sau truyền.
Sau khi được nuôi cấy và nhân lên ex vivo, các tế bào CAR-T được truyền trở lại cơ thể, nơi chúng nhận diện và tiêu diệt các tế bào đích mang kháng nguyên tương ứng bằng cơ chế phóng thích perforin, granzyme và các cytokine gây độc tế bào. Điểm ưu việt của cơ chế này là không phụ thuộc vào trình diện kháng nguyên qua MHC, giúp CAR-T vượt qua một trong những hàng rào lớn nhất trong điều trị miễn dịch truyền thống (Li et al., Nature Reviews Cancer, 2025).
Trên lâm sàng, CAR-T cell đã chứng minh hiệu quả vượt trội trong các bệnh bạch cầu lympho cấp dòng B (ALL), lymphoma tế bào B lớn tái phát hoặc kháng trị (R/R DLBCL), và đa u tủy xương (multiple myeloma).
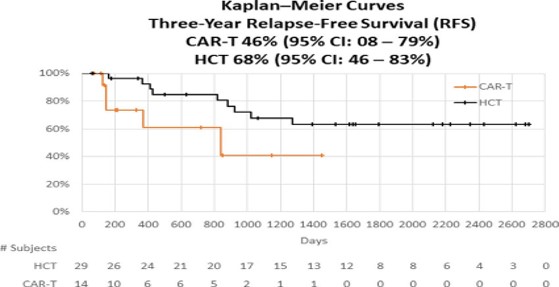
Biểu đồ Kaplan–Meier về tỷ lệ sống toàn bộ (OS) và sống không tiến triển bệnh (PFS) ở bệnh nhân ung thư dòng tế bào B tái phát hoặc kháng trị được điều trị bằng liệu pháp CAR-T cell.
Nhiều nghiên cứu cho thấy tỷ lệ đáp ứng toàn phần (CR) dao động từ 40–80% ở nhóm bệnh nhân R/R DLBCL, trong khi thời gian sống không tiến triển có thể kéo dài trên hai năm ở những bệnh nhân duy trì được quần thể tế bào CAR-T bền vững (Abramson, Blood Reviews, 2024). Biểu đồ Kaplan–Meier cho thấy liệu pháp CAR-T cell giúp cải thiện rõ rệt tỷ lệ sống toàn bộ (OS) và sống không tiến triển bệnh (PFS) ở bệnh nhân ung thư dòng tế bào B tái phát hoặc kháng trị. Sau thời gian theo dõi trung vị 24 tháng, tỷ lệ OS đạt 49,1% và PFS đạt 21,0%, cho thấy một phần đáng kể bệnh nhân duy trì đáp ứng lâu dài sau điều trị (Abramson, Blood Reviews, 2024).
Bên cạnh hiệu quả nổi bật, CAR-T cell cũng đi kèm các tác dụng không mong muốn đặc trưng, đòi hỏi sự giám sát nghiêm ngặt từ nhóm điều trị đa chuyên ngành. Phổ biến nhất là hội chứng giải phóng cytokine (Cytokine Release Syndrome – CRS), xảy ra ở khoảng 70–90% bệnh nhân, biểu hiện sốt cao, tụt huyết áp, rối loạn hô hấp và có thể dẫn tới suy đa cơ quan. Độc thần kinh liên quan miễn dịch (ICANS) là biến chứng đáng lo ngại thứ hai, biểu hiện rối loạn ý thức, co giật, phù não, đôi khi để lại di chứng thần kinh.
Ngoài ra, hiện tượng giảm miễn dịch kéo dài do mất tế bào B bình thường có thể làm tăng nguy cơ nhiễm trùng nặng. Hướng dẫn của ESMO (2025) và các nghiên cứu thực hành lâm sàng đều nhấn mạnh vai trò của tocilizumab (ức chế IL-6) và corticosteroid trong xử trí CRS/ICANS mức độ nặng, cùng với theo dõi sát và chăm sóc hỗ trợ toàn diện (Santomasso et al., Cancers, 2024).
Trên thế giới, đến năm 2025 đã có hơn 1.000 thử nghiệm CAR-T đang được triển khai, trong đó châu Á – đặc biệt là Trung Quốc, Hàn Quốc và Nhật Bản – nổi lên với năng lực tự sản xuất và chi phí thấp hơn 60–80% so với Mỹ hoặc châu Âu. Tuy nhiên, theo báo cáo của Springer Nature (2025), khả năng tiếp cận CAR-T ở khu vực Đông Nam Á vẫn còn rất hạn chế do chi phí cao, cơ sở hạ tầng kỹ thuật phức tạp và yêu cầu kiểm soát chất lượng nghiêm ngặt.
Tại Việt Nam, ca điều trị CAR-T đầu tiên đã được thực hiện thành công vào năm 2024. Các đơn vị, trong đó có Viện Huyết học – Truyền máu TW đang phối hợp quốc tế hướng tới sản xuất CAR-T “Made in Vietnam” với kỳ vọng tối ưu về chi phí (Journal of Military Pharmaco-Medicine, 2025).
Dù đã có những thành tựu ban đầu, khả năng tiếp cận CAR-T tại Việt Nam vẫn còn nhiều thách thức. Trước hết là chi phí điều trị cao, chưa được bảo hiểm y tế chi trả; thứ hai là hạn chế về cơ sở vật chất đạt chuẩn GMP để xử lý và nuôi cấy tế bào; và thứ ba là thiếu nhân lực chuyên sâu trong quản lý biến chứng miễn dịch nặng như CRS hay ICANS. Ngoài ra, quy trình logistic phức tạp (từ lấy mẫu, sản xuất, kiểm định đến truyền lại bệnh nhân) kéo dài hàng tuần, trong khi nhiều bệnh nhân ung thư máu tiến triển nhanh và không đủ thời gian chờ. Để mở rộng ứng dụng, cần có chính sách đầu tư và hành lang pháp lý rõ ràng cho liệu pháp tế bào, bao gồm đăng ký, kiểm nghiệm, giám sát an toàn sau điều trị và quy định chi trả phù hợp.
Tóm lại, CAR-T cell therapy là bước ngoặt mang tính cách mạng trong điều trị ung thư huyết học, với cơ chế miễn dịch chủ động và hiệu quả vượt trội so với các phương pháp truyền thống. Sự thành công của ca điều trị đầu tiên tại Việt Nam đánh dấu một mốc quan trọng, chứng minh năng lực nghiên cứu và ứng dụng công nghệ sinh học tiên tiến trong nước. Tuy nhiên, để CAR-T có thể trở thành một lựa chọn phổ biến, cần giải quyết đồng thời các vấn đề về chi phí, pháp lý, hạ tầng và nhân lực chuyên sâu. Việc nội địa hóa công nghệ, xây dựng hệ thống sản xuất tế bào đạt chuẩn GMP, cùng với chính sách hỗ trợ thanh toán y tế hợp lý sẽ là chìa khóa giúp bệnh nhân tại Việt Nam có thể tiếp cận rộng rãi hơn với liệu pháp đột phá này trong tương lai gần.
Khoa Dược
Viện Huyết học – Truyền máu TW
Tài liệu tham khảo (TLTK)
1. Abramson, S. (2024). CAR-T cell therapy for B-cell lymphomas: Progress and challenges. Blood Reviews, 68, 101–115.
2. ESMO Clinical Practice Guidelines. (2025). Management of CAR-T cell-related toxicities and clinical use recommendations. European Society for Medical Oncology. Retrieved November 2025.
3. Li, M., Chen, Y., & Wang, X. (2025). Advances in chimeric antigen receptor T-cell therapy for hematologic malignancies. Nature Reviews Cancer, 25, 1234–1250.
4. Santomasso, B. D., Park, J. H., & Neelapu, S. S. (2024). Neurotoxicity and cytokine release syndrome after CAR-T cell therapy: Mechanisms and management strategies. Cancers (Basel), 16(8),
5. Springer Nature. (2025). Improving access to CAR-T therapy in Asia: Regional challenges and policy implications. Springer Nature Insight Report. Retrieved November 2025.
6. Bộ Y tế. (2025). Thông cáo báo chí: Triển khai và quản lý liệu pháp tế bào CAR-T tại Việt Nam. Bộ Y tế Việt Nam.
7. Vinmec Research Institute of Stem Cells and Gene (2024). First successful application of CAR-T cell therapy in Vietnam. Vinmec Health System. Retrieved November 2025.
8. Zhang, H., Liu, Q., & Zhao, L. (2024). Emerging CAR-T cell therapies for solid tumors: Progress and perspectives. Scientific Archives.
9. Journal of Military Pharmaco-Medicine (JMPM). (2025). Domestic development of CAR-T cell technology in Vietnam. JMPM, 50(2), 45–52.
Bài viết liên quan
Bản tin thông tin thuốc số 01 – 2026
16 Tháng Một, 2026Bản tin thông tin thuốc do bộ phận Dược lâm sàng – Khoa Dược, Viện Huyết học – Truyền máu Trung ương biên soạn nhằm cập nhật thông tin cho…
Người bệnh có tiểu cầu thấp cần lưu ý đặc biệt khi dùng thuốc giảm đau
05 Tháng Hai, 2026Trong quá trình điều trị, người bệnh thường phải đối mặt với cơn đau do bệnh lý ác tính hoặc tác dụng không mong muốn khác. Thuốc giảm đau là…







