Nên tăng liều thuốc ức chế TKIs thế hệ 1 hay chuyển thế hệ 2 khi không đáp ứng điều trị bước 1?
Sự ra đời của thuốc ức chế TKIs (tyrosine kinase inhibitor) đã tạo ra một bước ngoặt trong lịch sử điều trị bệnh lý CML. Thuốc này đã giúp cho kết quả điều trị của người bệnh không những cải thiện về tiên lượng sống, thời gian sống thêm toàn bộ mà còn góp phần nâng cao chất lượng cuộc sống. Tuy nhiên, khi người bệnh không đáp ứng điều trị bước 1 thì nên tăng liều điều trị thuốc ức chế TKIs thế hệ 1 hay chuyển thế hệ 2?
Lơ xê mi kinh dòng bạch cầu hạt là một trong những bệnh máu thường gặp trong hội chứng tăng sinh tủy mạn ác tính. Đột biến trao đổi chéo giữa nhiễm sắc thể (NST) số 9 và 22 tạo thành nhiễm sắc thể số 22 mới (gọi là NST Philadelphia – Ph) mang gen lai BCR – ABL, được coi là cơ chế bệnh sinh chính của CML. NST Ph có mặt trên 95% người bệnh CML ở giai đoạn mạn tính. Gen BCR – ABL trong bệnh CML mã hóa tổng hợp protein 210KDa (P210) có hoạt tính tyrosin kinase nội sinh mạnh tham gia vào điều hòa sự phát triển của tế bào, đây là cơ sở cho việc nghiên cứu và ứng dụng các thuốc điều trị đích ức chế hoạt tính tyrosin kinase (TKI) của protein BCR – ABL1 [1].
Imatinib là thuốc ức chế TKIs thế hệ 1, được ra đời vào cuối những năm 1990. Qua quá trình nghiên cứu và thử nghiệm lâm sàng, năm 2001, Imatinib được FDA chấp thuận sử dụng tại Hoa Kỳ và được đưa ra thị trường.
Người bệnh dùng thuốc qua đường uống tại nhà, theo dõi và thăm khám định kỳ. Họ không cần nằm viện điều trị nội trú. Họ có thể có cuộc sống sinh hoạt, khả năng làm việc… gần như những người bình thường.
Trong quá trình dùng thuốc, người bệnh được bác sĩ thăm khám và theo dõi định kỳ bằng cả triệu chứng lâm sàng và xét nghiệm. Trong đó, xét nghiệm đặc biệt quan trọng giúp đánh giá kết quả điều trị và theo dõi đáp ứng thuốc là xét nghiệm định lượng gen BCR – ABL mỗi 3 đến 6 tháng tùy theo khuyến cáo.
Từ đó, các Hiệp hội Ung thư Thế giới như Mạng lưới Ung thư Quốc gia Mỹ (NCCN – National Comprehensive Cancer Network) hay Hiệp hội Ung thư Châu Âu (ELN – European Leukemia Network) sẽ đưa ra các khuyến cáo cụ thể ở từng mốc thời gian 3 tháng, 6 tháng, 12 tháng hay thời điểm bất kỳ…. để đánh giá người bệnh còn đáp ứng thuốc không [2].
Người bệnh được xếp loại vào các vùng an toàn, cảnh báo hay thất bại điều trị. Từ đó, người bệnh sẽ được theo dõi sát sao, kịp thời đưa ra kế hoạch điều trị tiếp theo để ngăn chặn bệnh tiến triển.
Khi phát hiện bệnh nhân thất bại với điều trị hàng 1, cần tăng liều Imatinib hay chuyển đổi thế hệ 2?
Theo khuyến cáo điều trị của NCCN năm 2022, dựa vào kết quả định lượng gen BCR – ABL của người bệnh tại các thời điểm, người bệnh sẽ được xếp loại vào các nhóm như sau:
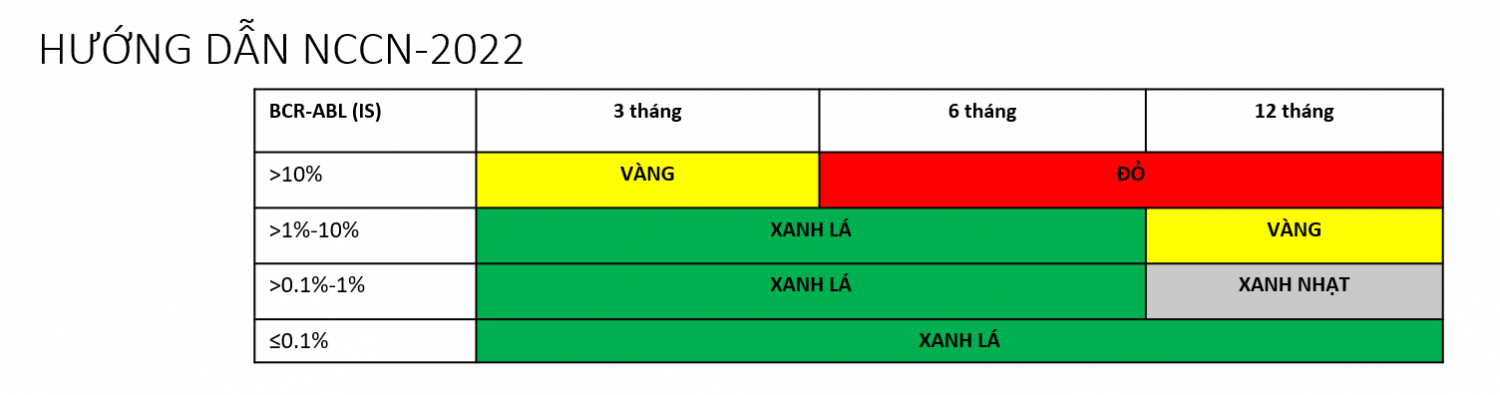
Từ việc đánh giá được chính xác đáp ứng điều trị của từng người bệnh, NCCN cũng đưa ra khuyến cáo tiếp theo. Khi người bệnh thuộc vùng cảnh báo màu vàng, tức là có nguy cơ sẽ mất đáp ứng với liều Imatinib x 400 mg/ngày thì có thể tăng liều cho người bệnh lên 800 mg/ngày hoặc chuyển TKIs thế hệ sau hoặc nghiên cứu chỉ định ghép tế bào gốc đồng loài [3].
Theo khuyến cáo điều trị của NCCN năm 2023, nhóm người bệnh thuộc vùng cảnh báo đã không còn chỉ định tăng liều thuốc thế hệ 1 mà chuyển đổi luôn sang thuốc thế hệ 2 [4] .
Điều này cũng được sự đồng thuận của nhiều hội ung thư khác trên thế giới như Hiệp hội Ung thư Châu Âu (ELN) [5], hay Hiệp hội Nội khoa Ung bướu Châu Âu (ESMO – European Society for Medical Oncology) [6].

Tại sao lại có sự thay đổi như vậy?
Kết quả của một số nghiên cứu lâm sàng trên thế giới đã chỉ ra rằng: liều cao Imatinib không giúp cải thiện thêm đáp ứng điều trị cũng như thời gian sống thêm cho người bệnh. Thay vào đó là vấn đề không dung nạp với thuốc.
Các tác dụng phụ không phải huyết học như đau xương khớp, buồn nôn, tiêu chảy, sốt, phù, suy giảm chức năng gan, thận, biến chứng tim mạch… sẽ tăng lên.
Tác dụng phụ về huyết học như giảm số lượng hồng cầu, bạch cầu, tiểu cầu cũng sẽ gặp tỷ lệ cao hơn khi sử dụng liều cao Imatinib. Lúc này, người bệnh sẽ có nguy cơ bị thiếu máu, xuất huyết chảy máu nặng nếu như tiểu cầu giảm thấp [7],[8],[9].
Bên cạnh vấn đề dung nạp thuốc, theo nghiên cứu LASOR năm 2016, khi so sánh kết quả điều trị giữa một nhóm người bệnh sử dụng thuốc Imatinib với liều cao 600 mg/ngày và nhóm người bệnh được sử dụng thuốc ức chế TKIs thế hệ 2 là Nilotinib, các tác giả đã nhận thấy: nhóm người bệnh dùng Nilotinib có tỷ lệ đạt đáp ứng về di truyền tế bào sau 6 tháng điều trị là cao hơn nhóm dùng liều cao Imatinib. Cụ thể là 48% so với 34%, đặc biệt trong đó có tới 6% người bệnh khi không đáp ứng với Imatinib đã phải chuyển sang nhánh dùng Nilotinib và cũng đã đạt được đáp ứng di truyền tế bào sau đó 6 tháng.
Tương tự khi đánh giá đáp ứng phân tử sâu (MMR -), nhóm người bệnh dùng Nilotinib sau 12 tháng đã đạt MMR với tỷ lệ gấp đôi so với nhóm sử dụng liều cao Imatinib (35% so với 16%) [10]. Điều này cũng đã được chỉ ra tương tự trong nghiên cứu ENESTcmr được thực hiện năm 2019 tại Thụy Sĩ [11] .
Dựa vào những kết quả thực tiễn rất thuyết phục và có giá trị khoa học trên, trong thực hành lâm sàng tại Việt Nam, Hướng dẫn chẩn đoán và điều trị một số bệnh lý huyết học năm 2022 của Bộ Y tế [12] cũng đã đưa ra khuyến cáo: nếu xuất hiện tình trạng kháng imatinib có thể sử dụng các thuốc ức chế hoạt tính tyrosin kinase thế hệ 2, hoặc ghép tế bào gốc tạo máu đồng loài.
Như vậy, tính đến thời điểm hiện tại, khi người bệnh gặp tình trạng mất đáp ứng với thuốc TKIs thế hệ 1 thì không còn chỉ định tăng liều thuốc. Người bệnh sẽ chuyển đổi sang các thuốc thế hệ 2. Việc này sẽ giúp cho việc điều trị đạt kết quả tối ưu do đạt được đáp ứng phân tử sâu. Từ đó sẽ ngăn chặn nguy cơ bệnh tiến triển hoặc chuyển dạng cấp tính. Tiên lượng sống còn cũng như chất lượng cuộc sống của người bệnh sẽ được cải thiện đáng kể.
ThS.BS. Nguyễn Thu Chang
Khoa Điều trị hóa chất
Viện Huyết học – Truyền máu TW
Tài liệu tham khảo:
1. M. Talpaz, R. T. Silver, B. J. Druker và cộng sự (2002). Imatinib induces durable hematologic and cytogenetic responses in patients with accelerated phase chronic myeloid leukemia: results of a phase 2 study. Blood, 99 (6), 1928-1937.
2. M. Baccarini, M. W. Deininger, G. Rosti và cộng sự (2013). European LeukemiaNet recommendations for the management of chronic myeloid leukemia: 2013. Blood, 122 (6), 872-884.
3. Referenced with permission from the NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) for Guideline Name V.1.2022.
4. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) for Guideline Name V1.2023
5. Baccarani M, et al. European LeukemiaNet recommendations for the management of chronic myeloid leukemia: 2013. Blood. 2013;122(6):872-884.
6. Hochhaus A, et al. Chronic myeloid leukemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2017;28:iv41-iv51.
7. Baccarani M, et al. Int J Hematol. 2014;99:616-624.
8. Baccarani M, et al. Blood. 2009;113:4497-4504.
9. Hehlmann R, et al. J Clin Oncol. 2011;29:1634-1642.
10. Cortes JE, et al. Lancet Haematol. 2016;3:e581-e591.
11. G-CML-1211381. Evolving Treatment Paradigms in CML. An Overview of the 2nd-Generation TKI Pivotal Trials. Basel, Switzerland: Novartis Pharma AG; April 2019.
12. Hướng dẫn chẩn đoán và điều trị một số bệnh lý huyết học (Ban hành kèm theo Quyết định số 1832/QĐ-BYT, ngày 01 tháng 07 năm 2022 của Bộ trưởng Bộ Y tế).
Tài liệu này được xây dựng với sự hỗ trợ của Novartis.
Bài viết liên quan
Lơ xê mi kinh dòng bạch cầu hạt: Nguyên nhân, triệu chứng và chẩn đoán
30 Tháng Một, 2024Lơ xê mi kinh dòng bạch cầu hạt (Chronic myeloid leukemia – CML) là một bệnh máu thường gặp, chiếm 5% tổng số các bệnh tạo máu và 20-25% các…
Phương pháp điều trị Lơ xê mi kinh dòng bạch cầu hạt
29 Tháng Ba, 2024Hiện có nhiều phương pháp điều trị lơ xê mi kinh dòng bạch cầu hạt. Đối với mỗi trường hợp, bác sĩ sẽ có phác đồ điều trị khác nhau…
Khi nào nên chuyển đổi điều trị lơ xê mi kinh dòng bạch cầu hạt?
30 Tháng Bảy, 2024Bệnh Lơ xê mi kinh dòng bạch cầu hạt (CML) là bệnh thuộc hội chứng tăng sinh tủy mạn ác tính, chiếm khoảng 0,2% bệnh lý ung thư nói chung…